 |
Zur Startseite von forum-stimme.de Übersicht über eine Vielfalt von Themen im Bereich der menschlichen Stimme |
 |
Heinz Stolze, Institut für Stimme und Kommunikation, Bremen
in www.forum-stimme.de
neu erstellt am 5.4.2002, überarbeitet am 9.7.2007
Luft - molekular - Ein Einblick in die molekulare Struktur der Luft
1 Luft und Stimme
Die Luft ist das Medium in dem die menschliche Stimme sich ausbildet und ausbreitet. Der Luftdruck der Lunge treibt die Schwingung der Stimmlippen im Kehlkopf an, die Luft im Vokaltrakt bildet ein Schwingungssystem, das die Stimmproduktion wesentlich bestimmt und die Luft außerhalb des Menschen trägt den Stimmschall weiter. Üblicherweise betrachtet man die Stimmmechanismen unter dem Aspekt, wie sie die Schallwelle in der Luft formen. Es ist aber auch interessant sich vorzustellen, wie die mechanisch-akustischen Eigenschaften der Luft ganz erheblich die Entwicklung der Stimmorgane mitgeprägt haben.
Um die Stimmproduktion zu verstehen, ist es jedenfalls nötig, einige Eigenschaften der Luft zu kennen. In Anbetracht der Bedeutung des Mediums Luft für die Stimme widmen wir der Luft einen Blick durch ein gedachtes "Supermikroskop", mit dem sich Moleküle beobachten lassen.
2. Ein mikroskopisches Modell der Luft
Luft besteht aus Gasmolekülen, ca 21% davon sind Sauerstoffmoleküle (O2) und 78% Stickstoffmoleküle (N2), ca 1% weitere Molekülarten. Der Einfachheit halber stellen wir uns nur eine Molekülsorte vor und zwar als Kügelchen, die im wesentlichen auf geraden Bahnen fliegen, bis sie auf ein anderes Molekül oder eine Wand treffen. Wenn zwei Moleküle aufeinanderprallen, stoßen sie sich wie zwei elastische Kugeln. Nach dem Stoß fliegt jedes in eine neue Richtung weiter. Dies ist das Modell eines "Idealen Gases", Abb. unten. Die Anziehungskraft zwischen den Molekülen wird hier insofern vernachlässigt, als gerade Bahnen zwischen den Stößen angenommen werden.
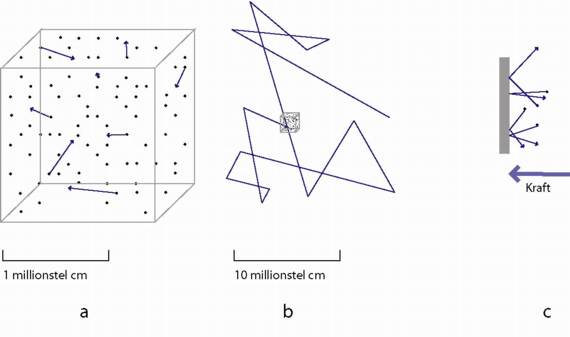
a: Moleküle in Bewegung. Bei einigen ist ihre Geschwindigkeit als blauer Pfeil dargestellt.
b: Typischer Weg eines Moleküls in zehnfach geringerer Vergrößerung als Teilbild a
c: Kraftwirkung auf eine Wand durch molekulare Stöße
Stellen Sie sich vor, daß die einzelnen Moleküle in Abb.a sich im freien Flug geradeaus bewegen. Ab und zu stoßen sie auf ein anderes Molekül und fliegen nach dem Stoß in eine andere Richtung weiter. Wenn Sie die Abbildung nicht flächig sondern dreidimensional auffassen, werden sie erkennen, daß die Wahrscheinlichkeit, daß eine Molekül ein anderes in diesem Würfel trifft, recht klein ist. In Abbildung b ist um den Faktor 10 zurückgezoomt, so daß auch ein typischer Molekülweg mit Stößen darstellbar ist. Er erscheint als eine ziemlich ungeordnete Zick-Zack-Bewegung (Brown´sche Bewegung).
Anmerkung "genaugenommen": Genaugenommen bewegt sich ein Körper in einem homogenen, konstanten Gravitationsfeld (das liegt für die Moleküle auf der Erdoberfläche vor) auf parabelförmigen Bahnen. Die meisten Moleküle sind aber so schnell und stoßen nach so kurzer Flugzeit wieder auf ein anderes, daß diese kurzen Wegstrecken für fast alle Moleküle als gerade Strecken angesehen werden können. Die Krümmung der auf sichtbare Größe vergrößerten Flugbahn wäre mit bloßem Auge nicht erkennbar. Die Geschwindigkeit eines einzelnen Moleküls ändert sich bei jedem Stoß, ist also mal größer, mal kleiner. Sie kann durchaus auch einmal so klein werden, daß die Bahn zwischen zwei Stößen erkennbar von einer Gerade abweicht. Dies ist aber derart selten, daß es für Berechnungen des Verhaltens von Gasen praktisch keine Rolle spielt.
Einige ungefähre Daten mögen die Größenordnungen des molekularen Geschehens veranschaulichen. Sie gelten für Luft bei Zimmertemperatur und Normaldruck.
Beim Stoß wirksamer Moleküldurchmesser: 0, 000 000 02 cm
Zahl der Moleküle pro Kubikzentimeter: 30 Milliarden Milliarden = 30 000 000 000 000 000 000
Statistischer Mittelwert für die Länge des Fluges zwischen zwei Stößen: 0,00002 cm
Mittlere Geschwindigkeit eines Moleküls: 50000 cm/sec oder 1800 km/h
Mittlere Zeitdauer zwischen zwei Stößen: 0,2 Milliardstel sec
Wenn Moleküle auf eine Wand stoßen, werden sie reflektiert, und es wirkt kurzzeitig eine Kraft auf die Wand. In unregelmäßiger Folge prallen Moleküle auf. Bei Zimmertemperatur und Normaldruck circa 600 000 Milliarden mal pro Sekunde und Quadratzentimeter. Im Makroskopischen, also etwa beim Fühlen mit der Haut oder Messen mit einem Manometer scheint ein konstanter Druck vorzuliegen, die einzelnen "Mikroschläge" sind nicht wahrnehmbar. Der Druck ist umso höher ist, je schneller die Teilchen fliegen und je häufiger eines die Wand trifft. Die Geschwindigkeit der Moleküle ist nach einem bestimmten statistischen Muster verteilt. Je höher die Temperatur ist, umso größer ist die mittlere Fluggeschwindigkeit und somit die Stoßkraft und der Druck. Bei konstanter Temperatur gilt: je dichter die Teilchen sind, umso mehr Stöße gegen die Wand finden statt und umso höher ist der Druck.
3. Luftdruck
Der Luftdruck ist eine zentrale Größe bei der Beschreibung der Stimmfunktion.
Auf der Erdoberfläche lastet im Mittel ein Druck von einer Atmosphäre. Dies entspricht in der international üblichen Druckeinheit Pascal 101 300 Pa oder 101,3 kPa (Kilopascal). Man kann sich vorstellen, daß die gesamte Luft der Atmosphäre von der Gravitationskraft der Erde angezogen wird. Dieses Gewicht äußert sich als Luftdruck auf der Erdoberfläche. Direkt über der Erde ist das Gewicht der gesamten Luft der Atmosphäre wirksam, entsprechend hoch ist der Druck und die Dichte der Luft. In höheren Schichten ist die Menge der darüberliegenden Luft geringer, dementsprechend geringer sind Luftdruck und Luftdichte. Würde man sich alle Luft der Atmosphäre mit derselben Dichte vorstellen, wie sie direkt auf der Erdoberfläche herrscht, so stünde über der Erde eine etwa 8 Km hohe Luftsäule .
Eine Wassersäule, die denselben Druck auf die Erdoberfläche ausübt wie diese Luftsäule, müsste eine Höhe von 10,33 m haben, eine Quecksilbersäule müsste 760 mm hoch sein. Drucke werden noch heute mit Manometern gemessen, in denen Wasser- oder Quecksilbersäulen benutzt werden. Wir verwenden im folgenden durchweg die Einheit Kilopascal, für die annähernd gilt: 100 kPa= 1 atm (Atmosphäre). Man kann sich bequem merken:1 kPa ist rund 1% einer Atmosphäre und entspricht in etwa dem Maß 10 cm Wassersäule.
Bei der Angabe von Drucken ist es oft praktisch, nicht den absoluten Wert anzugeben, sondern die Abweichung von einem festliegenden Referenzwert. Man nennt solche Angaben relative Druckwerte. Normalerweise bezieht man den Druck in Behältern auf den herrschenden Außendruck, die Differenz beider Werte ist der relative Druck (positiv bei Überdruck, negativ bei Unterdruck). In der Lunge ist der relative Druck während des Einatmens negativ, während des Ausatmens positiv. Um ein Gefühl für relative Druckwerte zu vermitteln, werden im folgenden einige typische Werte angegeben. Der Referenzdruck, auf den sich die Angabe bezieht, ist jeweils angegeben.
10000 m Höhe: - 68 kPa (bezogen auf den Druck auf der Erdoberfläche)
(Reisehöhe kommerzieller Düsenflugzeuge)
Nach der Faustregel "ein kPa ist rund 1% einer Atmosphäre" herrscht also ein Druck entsprechend einem Abzug (Minuszeichen vor 68 kPa) von 68%, oder anders gesagt: der Druck beträgt nur 32 % des Druckes auf der Erdoberfläche.
1000 m Höhe: -10 kPa (bezogen auf den Druck auf der Erdoberfläche)
Lunge: maximaler Druck circa: 10 kPa (bezogen auf den Außendruck)
Lunge: bei lautem Singen ca: 3 kPa, bis zu circa 6 kPa möglich
ausgeprägtes Hochdruckgebiet circa: 2 kPa (bezogen auf den mittleren Luftdruck über lange Zeit)
ausgeprägtes Tiefdruckgebiet circa: -2 kPa (bezogen auf den mittleren Luftdruck über lange Zeit)
Lunge: bei mäßig lautem Sprechen circa: 1 kPa (bezogen auf den Außendruck)
Schalldruck bei lautem Singen circa : 0,002 kPa (im Moment des stärksten Ausschlages)
in 0,5 m Abstand vom Mund (100 dB), (bezogen auf den Außendruck bei absoluter Stille)
Schalldruck bei lautem Sprechen circa 0,0002 kPa (im Moment des stärksten Ausschlages)
in 0,5 m Abstand vom Mund:(80 dB),(bezogen auf den Außendruck bei absoluter Stille)
Fragen und Anregungen bitte an den Autor: E-Mail